Hauptunterschied: Die Atommasse ist einfach die Masse eines bestimmten Isotops oder die kombinierte Masse der Protonen, Neutronen und Elektronen des Atoms. Die Ordnungszahl ist die Anzahl der Protonen, die sich in einem Elementkern befinden.
Betrachten wir die Chemie als verwirrend, die verschiedenen Elemente, Ordnungszahlen, Bindungen, Masse, Gewicht, Atome usw. All diese Wörter verschwimmen nach einer bestimmten Zeit, die eine Person nicht mehr voneinander unterscheiden kann. Nun, Atommasse und Ordnungszahl sind zwei solcher Wörter, die oft verwirrt und austauschbar verwendet werden.
Die Atommasse ist die Masse eines Atoms im Ruhezustand. Dies liegt daran, dass wenn ein Atom sich mit einer sehr hohen Geschwindigkeit bewegt, seine Masse zunimmt. Obwohl die Atommasse laut Definition die Masse aller Protonen, Neutronen und Elektronen ist, sind Elektronen zu klein, um einen signifikanten Unterschied in der Atommasse zu bewirken. Die meisten Elemente des Periodensystems enthalten Isotope und aufgrund des Unterschieds in der Neutronenzahl ändert sich auch die Masse jedes Isotops.
Die Atommasse wird in Atommasseneinheiten oder amu ausgedrückt. Eine Atommasseneinheit entspricht 1/12 der Masse von Kohlenstoff-12. Wenn die Masse eines Atoms durch 1/1 der Masse von Kohlenstoff-12 geteilt wird, wird die relative Masse des Elements erhalten. Die relative Masse eines Objekts ist jedoch tatsächlich das Atomgewicht eines Elements, da es berechnet wird, indem alle Isotope betrachtet werden. Dies sollte jedoch nicht als Atommasse eines Elements angenommen werden.

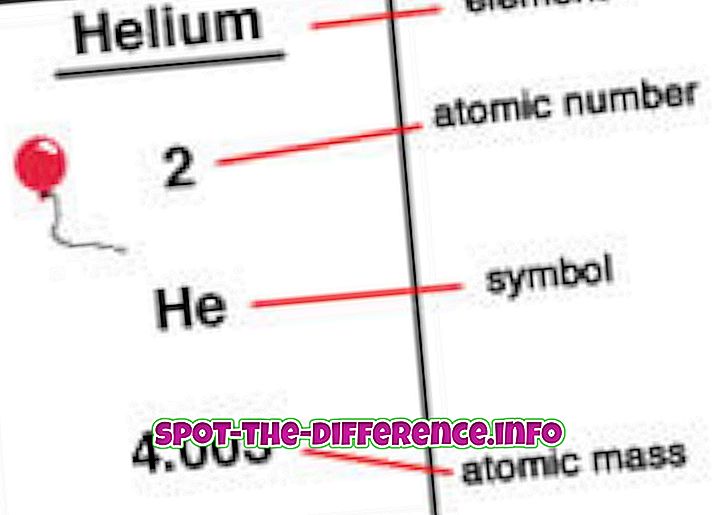
Die Ordnungszahl ist die Anzahl der Protonen, die sich in einem Elementkern befinden. Wenn ein Atom neutral ist, bedeutet dies, dass es die gleiche Anzahl von Protonen und Elektronen hat. Die Ordnungszahl wird mit einem Z bezeichnet. Da jedes Element eine andere Anzahl von Protonen aufweist, wird diese Anzahl auch zur Darstellung eines Elements verwendet. Isotope haben normalerweise die gleiche Ordnungszahl, werden aber nach ihrer Atommasse klassifiziert, beispielsweise Kohlenstoff-12, Kohlenstoff-13.
Elemente werden in der Reihenfolge der Ordnungszahlen in einem Periodensystem angeordnet. Die Ordnungsnummer ist in der linken oberen Ecke des Elements als hochgestellt aufgeführt. Atomnummern können helfen, Informationen über das Element preiszugeben, und viele Leute können die Ordnungszahl sehen und angeben, um welches Element es sich handelt. Es zeigt auch an, wo im Periodensystem es platziert werden kann und ob es flüssig, gasförmig oder fest ist. Die Ordnungszahl gibt auch Auskunft über Kernladung, Oxidationszustände, Bindungsverhalten, Ladung des Ions usw.