Hauptunterschied: Eine ionische Bindung ist eine chemische Bindung zwischen zwei verschiedenen Atomen (dh einem Metall und einem Nichtmetall), bei denen ein Atom ein Elektron an ein anderes abgibt. Eine kovalente Bindung ist eine weitere starke chemische Bindung. Es findet ähnliche Atome (dh zwei Nichtmetalle) statt. In einer kovalenten Bindung kommen die beiden Atome zusammen, um das Elektron zu teilen, anstatt dass ein Atom ein Elektron von einem anderen nimmt.
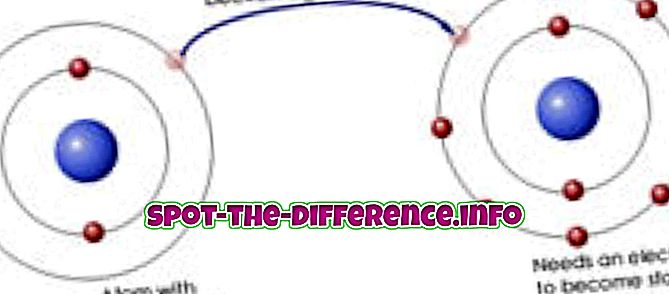
Eine ionische Bindung ist eine chemische Bindung zwischen zwei verschiedenen Atomen (dh einem Metall und einem Nichtmetall), bei denen ein Atom ein Elektron an ein anderes abgibt. Daher werden beide Atome zu Ionen, da ein Atom ein Elektron weniger hat, während das andere ein Extra hat. Das Metallion, das ein Elektron verloren hat, hat eine positive Ladung. Das Nichtmetallion, das ein Elektron gewonnen hat, hat eine negative Ladung. Wenn sich Gegensätze anziehen, werden diese Ionen dann so stark angezogen, dass sie sich verbinden.
Ionische Verbindungen liegen üblicherweise in Form von Feststoffen, dh Salzen vor. Sie sind in Wasser gut löslich und haben einen hohen Schmelzpunkt. Wenn sie sich im Wasser befinden, haben sie auch eine hohe elektrische Leitfähigkeit.

Die kovalente Bindung umfasst viele Arten von Wechselwirkungen, einschließlich σ-Bindung, π-Bindung, Metall-Metall-Bindung, agostische Wechselwirkungen und Dreizentren-Zwei-Elektronen-Bindungen. Wenn ein Atom ein Elektron in seiner äußeren Hülle hat und ein anderes Atom ein Elektron benötigt, um seine äußere Hülle zu füllen, dann teilen die beiden Atome das Elektron gemeinsam. Somit haben beide Atome eine vollständige äußere Hülle und entsprechend eine stabile elektronische Konfiguration.
Chemische Bindungen werden so hergestellt, dass das Atom eine vollständige äußere Hülle haben kann, da eine volle äußere Hülle eine stabile elektronische Konfiguration bedeutet. Wenn in einer ionischen Bindung das Metallatom ein einzelnes Elektron in seiner äußeren Hülle hat und das Nichtmetall ein Elektron benötigt, um seine äußere Hülle zu vervollständigen, gibt das Metallatom sein Elektron an das Nichtmetall ab. In ähnlicher Weise teilen sie in der kovalenten Bindung das Elektron gleich.
Ionenverbindung | Kovalente Bindung | |
Definition | Eine chemische Bindung zwischen zwei ungleichen Atomen, in der ein Atom ein Elektron an ein anderes abgibt. | Eine kovalente Bindung ist eine chemische Bindung, bei der Elektronen zwischen zwei ähnlichen Atomen geteilt werden. |
Auftreten | Ein Metall und ein Nichtmetall | Zwei Nichtmetalle |
Polarität | Hoch | Niedrig |
Form des Moleküls | Keine bestimmte Form, Gitterstrukturen | Bestimmte Form |
Elektrische Leitfähigkeit | Hoch | Normalerweise keine |
Wärmeleitfähigkeit | Hoch | Normalerweise niedrig |
Schmelzpunkt der Substanz | Variiert, aber normalerweise höher als kovalente Verbindungen | Variiert, aber normalerweise niedriger als ionische Verbindungen |
Siedepunkt der Substanz | Hoch | Variiert, aber normalerweise niedriger als ionische Verbindungen |
Löslichkeit in Wasser | Hoch | Variiert, aber normalerweise niedriger als ionische Verbindungen |
Stoffzustand bei Raumtemperatur | Normalerweise fest | Festes Flüssiggas |