Hauptunterschied : Die Absorption ist ein Massenphänomen, bei dem ein Absorbat vollständig in den Körper eines Feststoffs oder einer Flüssigkeit eindringt, um eine Verbindung oder eine Lösung zu bilden. Andererseits ist Adsorption ein Oberflächenphänomen, bei dem sich Moleküle eines Adsorbats nur auf der Oberfläche eines Adsorbens konzentrieren.
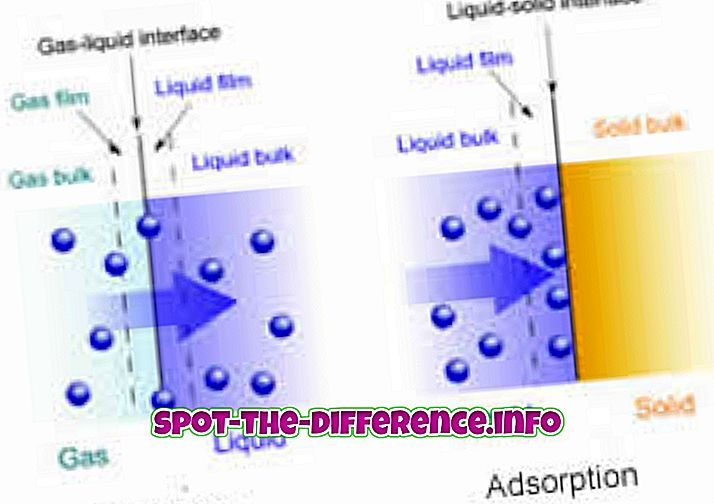
Chemische Reaktion - Kohlendioxid, das von einer Kaliumkohlenstofflösung absorbiert wird
Physikalischer Prozess - Durch Auflösen in Wasser absorbierte Luft

Es gibt zwei Arten von Adsorptionsmodi - chemische und physikalische. Bei der chemischen Adsorption werden die Moleküle und die Oberfläche durch schwache Vander Walls-Kräfte gebunden. Andererseits wird bei der chemischen Adsorption eine chemische Bindung zwischen Molekülen und Oberfläche gebildet.
Daher besteht der Hauptunterschied zwischen Adsorption und Absorption darin, dass die Absorption ein Massenphänomen ist, was bedeutet, dass sie im gesamten Körper des Materials vorkommt, während die Adsorption ein Oberflächenphänomen bleibt. Die Adsorption ist immer exotherm, während die Absorption endotherm ist. Sorption umfasst sowohl Absorptions- als auch Adsorptionsprozesse.
Vergleich zwischen Adsorption und Absorption:
Adsorption | Absorption | |
Definition | Ansammlung eines gelösten Gases oder einer Flüssigkeit auf der Oberfläche eines Feststoffs oder einer Flüssigkeit | Diffusion einer Substanz in eine Flüssigkeit oder einen Feststoff zur Bildung einer Lösung oder Verbindung |
Beispiel | Inertgase werden auf Holzkohle adsorbiert. | Ein trockener Schwamm nimmt Wasser auf |
Wärmeaustausch | Exotherm mit Ausnahme der Adsorption von H2 an Glas | Endothermisch |
Gleichgewicht erreichen | Vergleichsweise schneller | Vergleichsweise langsam |
Konzentration | Die Konzentration auf der Oberfläche des Adsorbens unterscheidet sich von der in der Masse | Die Konzentration bleibt im gesamten Material gleich |
Häufigkeit des Auftretens | Anfangs ist es schnell, aber später sinkt die Rate | Es findet zu einheitlichen Preisen statt |